DISCLAIMER — Not financial advice. Educational content only, not an offer or solicitation to buy or sell any security. Biotech and small/mid-cap stocks are highly speculative and volatile and can result in a partial or total loss of capital. Do your own research and consult a licensed advisor where appropriate. / Contenuti a solo scopo informativo e didattico, non costituiscono consulenza finanziaria né offerta o sollecitazione al pubblico risparmio ai sensi delle normative CONSOB e SEC. Le azioni biotech e le small/mid cap sono strumenti altamente speculativi e volatili e possono comportare la perdita parziale o totale del capitale investito. Si raccomanda di effettuare sempre le proprie ricerche e, se necessario, di rivolgersi a un consulente abilitato.

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker

Merlintrader Trading Pub
Biotech catalyst news and analysis. FDA PDUFA tracker
Merlintrader Deep Dive • Biotech / Clinical-Stage
Revelation Biosciences, Inc. (Nasdaq: $REVB): Gemini, AKI, CKD and the High-Risk Micro-Cap Repricing Setup
A mirrored EN/IT deep dive on Revelation Biosciences, its Gemini platform, the FDA-aligned AKI pathway, PRIME CKD data, cash runway, dilution history, reverse split risk and the speculative catalyst map into 2026.
Next Catalyst Watch: the most important operational catalyst is the formal initiation and execution path of the planned adaptive Phase 2/3 GEM-AKI trial. Revelation has stated that it is building the required infrastructure during 2026, including CRO engagement, advisory input and clinical drug supply, after reaching agreement with the FDA on a single adaptive Phase 2/3 design for AKI.
Company
Clinical-stage biotech
Lead asset
Gemini / PHAD®
Core target
TLR4 / innate immunity
Key risk
Dilution + execution
Executive Summary
Revelation Biosciences, Inc. (NASDAQ: REVB) is a clinical-stage biopharmaceutical company based in San Diego, California, focused on developing innovative therapies built around modulation of the innate immune system. Its lead product candidate, Gemini, is a proprietary intravenous formulation of PHAD® (phosphorylated hexaacyl disaccharide), a Toll-like receptor 4 agonist designed to “reprogram” or rebalance innate inflammatory response in order to prevent or reduce organ damage associated with acute and chronic inflammation.
2025 and early 2026 represented a major inflection period for the company. Revelation reported positive completion of the PRIME Phase 1b study in chronic kidney disease patients, reached an important agreement with the FDA on the proposed approval pathway for Gemini in acute kidney injury, and formed a high-profile international Advisory Board for the planned pivotal adaptive Phase 2/3 trial. These developments moved Gemini from a narrow early-stage biomarker story toward a more defined clinical-regulatory pathway in an indication with substantial unmet need.
At the same time, REVB remains a very high-risk equity story. The company’s market capitalization is extremely small, the share price has lost nearly all of its value over the last year, and the company has completed repeated reverse stock splits over the past three years to maintain NASDAQ listing compliance. The financial structure is fragile, the need for additional capital remains material, and the planned AKI trial will require far greater execution capability than earlier Phase 1 or Phase 1b work.
For readers, the most important takeaway is that Revelation is not a simple “cheap cash box” and not a conventional de-risked biotech. It is a speculative clinical-stage micro-cap with a differentiated immune-modulation platform, promising early biomarker data, a potentially efficient FDA-aligned AKI pathway, and severe financing and dilution risk. The bull case depends on Gemini’s biology translating into hard clinical outcomes such as reduced death and/or dialysis. The bear case depends on the more familiar micro-cap biotech pattern: dilution, delays, regulatory friction, weak market confidence and another cycle of capital pressure.
1. Company Profile
Revelation Biosciences was incorporated in 2019 as Petra Acquisition, Inc. and adopted its current name in January 2022 following a SPAC merger. The company operates with an extremely lean structure and a business model typical of a clinical-stage biotechnology company: no approved products, no operating revenue and full dependence on external financing to support research, development, regulatory work and corporate operations.
The company is led by James M. Rolke, co-founder, Chief Executive Officer and Chairman, who has long experience in the biotechnology sector. Chester Stanley Zygmont III serves as Chief Financial Officer and Corporate Secretary. The internal employee base is very small, which helps keep the burn rate lower than it would be in a larger clinical organization, but also means that the company must rely heavily on CROs, outside consultants, scientific advisors, regulatory specialists, clinical sites and academic collaborators to move complex programs forward.
The company’s core technology has also been developed through collaboration with Vanderbilt University. In October 2022, Revelation entered into an exclusive worldwide license agreement with Vanderbilt for infectious disease applications of PHAD. This agreement supports the broader multi-indication story around Gemini and provides a scientific bridge toward post-surgical infections, hospital-acquired infections, post-burn infections and other contexts where immune dysregulation and innate immune response may influence clinical outcomes.
From an equity-market perspective, this profile creates a familiar but very sharp trade-off. Revelation is small enough that any credible clinical or strategic validation could matter disproportionately for valuation. But it is also small enough that capital formation, listing compliance and execution capacity remain constant issues. A company with a small team and no revenue cannot absorb clinical setbacks or weak financing conditions in the same way as a larger biotech or pharmaceutical sponsor.
| Feature | Detail |
|---|---|
| Headquarters | San Diego, California |
| Corporate history | Incorporated in 2019 as Petra Acquisition, Inc.; renamed Revelation Biosciences in January 2022 |
| Employees | Very lean structure; StockAnalysis reports 9 employees |
| CEO | James M. Rolke, co-founder, CEO and Chairman |
| CFO | Chester Stanley Zygmont III |
| Sector | Biotechnology / Healthcare |
| Lead product candidate | Gemini, proprietary PHAD® formulation |
| Key license | Vanderbilt University, October 2022, for infectious applications of PHAD |
2. Core Technology: Gemini and Mechanism of Action
The core of Revelation’s strategy is Gemini, a proprietary intravenous formulation of PHAD® (phosphorylated hexaacyl disaccharide). PHAD is a synthetic agonist of Toll-like receptor 4, a key receptor in innate immunity involved in recognition of danger signals associated with pathogens, tissue injury and biological stress.
The mechanism is built around the concept of trained immunity. Revelation’s thesis is that controlled stimulation of TLR4 with Gemini can rebalance innate immune cells, especially monocytes and neutrophils, shifting them away from a pathological inflammatory or immune-paralyzed state toward a more protective and controlled immune response. This is meaningfully different from classic broad immunosuppression. Rather than simply blocking immune activity, Gemini is intended to normalize and improve the quality of immune response to subsequent stressors such as ischemia, infection or trauma.
This is the key scientific reason Gemini is being explored across multiple indications. AKI, CKD, post-surgical infection and severe burn infection prevention are different clinical settings, but they share a common theme: inflammatory dysfunction, innate immune activation or immune paralysis can influence organ damage, infection risk and recovery. If Gemini can safely rebalance this system, the same product candidate may have platform-like optionality.
One important safety point from the early clinical data is selectivity of response. According to Revelation, Gemini did not produce significant increases in TNF-α at the highest tested dose and did not produce significant increases in IL-1β in the referenced Phase 1 dataset, while showing upregulation of protective or anti-inflammatory mediators such as IL-1RA, NGAL and IL-10. For a TLR4 agonist, this distinction matters because uncontrolled TLR4 activation could theoretically produce excessive inflammatory toxicity.
“The activity observed with a single dose of Gemini in patients is shocking. This effect suggests a meaningful step forward in addressing the underlying immune dysregulation observed in patients with chronic kidney disease.”Dr. Adam Horeish, MD, Principal Investigator, Balboa Research, as cited by Revelation Biosciences
The central unresolved question is not whether Gemini has a plausible mechanism. The unresolved question is whether biomarker activity and immune rebalancing can translate into clinically meaningful outcomes in AKI: fewer deaths, less dialysis, better renal recovery and improved hospital outcomes. That is the bridge the planned Phase 2/3 trial must attempt to build.
3. Clinical Pipeline
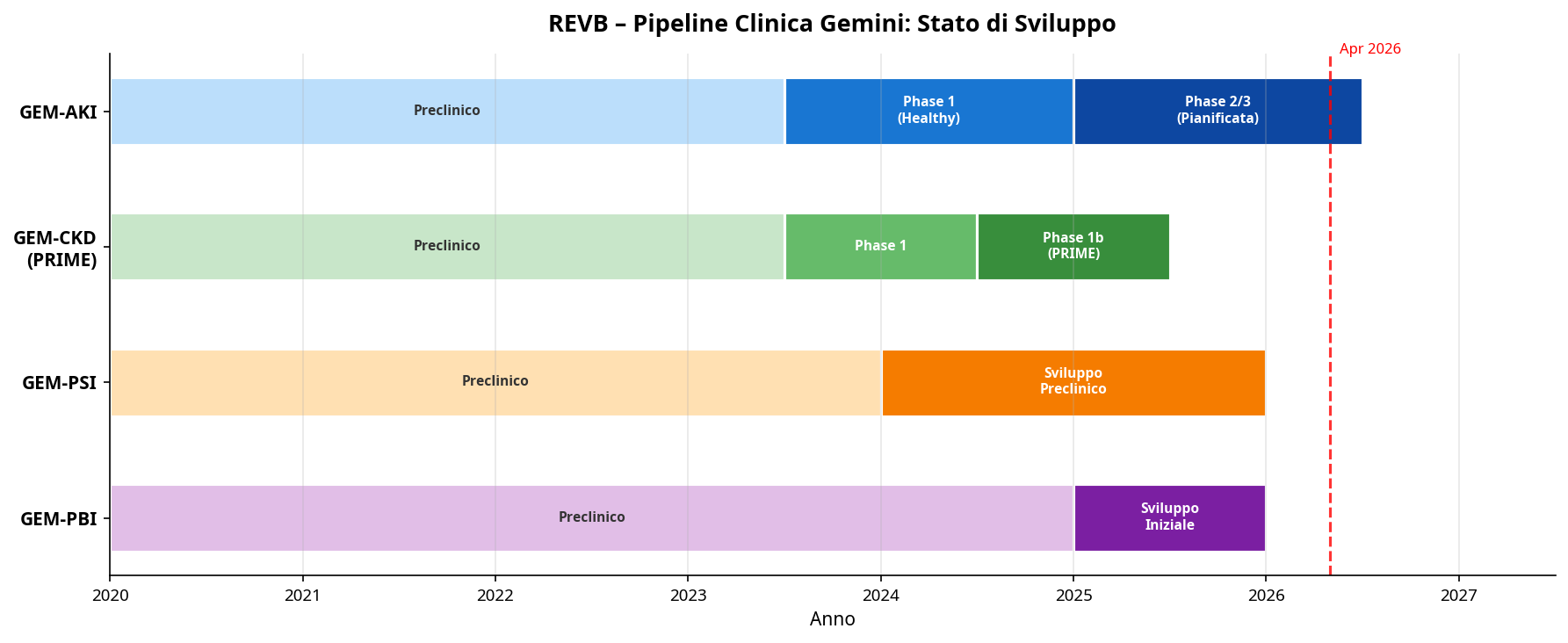
Revelation’s pipeline is built entirely around Gemini and applies the same innate immune rebalancing concept to four therapeutic areas. That concentration gives the story scientific coherence, but it also concentrates risk. If Gemini’s mechanism fails to produce clinically relevant results in AKI or CKD, the broader platform narrative would weaken quickly. Conversely, if the AKI program produces credible clinical evidence, the same platform may gain value across additional indications.
3.1 GEM-AKI — Acute Kidney Injury
GEM-AKI is the company’s most advanced and most important program. Acute kidney injury is characterized by a rapid decline in kidney function. It affects a large share of hospitalized patients and more than half of patients in intensive care settings according to the epidemiology cited by the company and third-party sources. Severe AKI can require dialysis, increase mortality, lengthen ICU stays and contribute to progression toward chronic kidney disease or end-stage renal disease.
In the United States, Revelation estimates approximately 6.8 million hospitalized AKI patients per year by applying an estimated 20% AKI incidence to roughly 34 million annual hospitalizations. The company also cites significant Medicare cost burden and severe clinical consequences, especially among patients who require dialysis. The most important commercial point is that there is still no broad pharmacologic therapy approved specifically to treat AKI across the general hospital population, with terlipressin representing a specific exception in the HRS-AKI subset.
On January 21, 2026, Revelation announced that it had reached agreement with the FDA on the proposed approval pathway for Gemini in AKI. Two elements are central. First, the FDA-aligned primary endpoint is a clinically meaningful composite of death and/or need for dialysis. Second, Revelation stated that positive data from a single adaptive Phase 2/3 study of approximately 300 patients could be sufficient to support submission of a New Drug Application.
The planned study design is split into two parts. Part 1 will evaluate different dosing regimens compared with placebo. Part 2 will proceed as the Phase 3 portion using the safest dosing regimen identified in Part 1. Data from both parts may be included in primary and secondary endpoint analyses. This is potentially valuable because it may compress the clinical development pathway and avoid a fully separate Phase 2 followed by a fully separate Phase 3. For a micro-cap company, that efficiency matters.
The limitation is that even a relatively efficient adaptive Phase 2/3 trial is not cheap or simple. AKI patients are clinically complex, hospital-based trials require strong site execution, and endpoint capture must be rigorous. Revelation will need trial infrastructure, CRO performance, drug supply, site activation, enrollment discipline, safety monitoring and enough capital to keep the program moving.
On April 6, 2026, Revelation announced the formation of an AKI Advisory Board including nephrology and critical care specialists from institutions such as Emory University, University of Alberta, University of Cincinnati/Cincinnati Children’s, UAB and University of Münster. This does not de-risk the trial by itself, but it does support protocol quality, clinical relevance and execution planning.
3.2 GEM-CKD — Chronic Kidney Disease and PRIME
GEM-CKD has completed the Phase 1b PRIME study in patients with stage 3 and stage 4 chronic kidney disease. The company reported that the study met its primary endpoint of safety and tolerability. Revelation also reported that more than 85% of patients had at least one elevated cytokine before treatment and that more than 60% had elevated IL-1β and IL-6 at baseline.
According to the company, Gemini significantly reduced the number of elevated cytokines at all measured timepoints through 7 days after a single dose compared with placebo. Revelation also reported normalization of background inflammation toward levels observed in healthy subjects, restoration of cellular response to stimulation and correction of the immune paralysis often observed in chronic disease. No serious adverse events were reported in the cited PRIME results, and adverse events at the target dose were described as mild.
The PRIME data are important because they create biological continuity between early safety work in healthy volunteers and the AKI pivotal concept. CKD is not AKI, and biomarker results do not equal approval-grade clinical outcomes. But PRIME suggests that Gemini can produce measurable immunologic activity in a real kidney disease population. That is why the market may treat additional PRIME presentations as supportive catalysts even though GEM-AKI remains the main value driver.
3.3 GEM-PSI — Post-Surgical Infection
GEM-PSI is being developed in collaboration with Vanderbilt University as a potential therapy for the prevention or treatment of hospital-acquired bacterial infections. The intended opportunity includes post-surgical infection, post-burn infection and urinary tract infection. The scientific basis is that systemic PHAD pretreatment has shown, in preclinical models cited by Revelation, significant reductions in the duration and severity of both gram-positive and gram-negative bacterial infection.
This program is strategically useful because it expands Gemini beyond kidney disease and reinforces the innate immune platform thesis. Commercially, however, it remains secondary until Revelation demonstrates that Gemini’s immune modulation can produce clinically meaningful outcomes in a more advanced program.
3.4 GEM-PBI — Severe Burn Infection Prevention
GEM-PBI was announced in April 2025 and is being developed for prevention of infection in patients with severe burns requiring hospitalization. This indication fits the platform logic: severe burn patients are vulnerable, immune response can become dysfunctional, infection risk is high and there may be a role for controlled immune priming or rebalancing.
Like GEM-PSI, GEM-PBI is earlier-stage and should be viewed as long-term optionality rather than a near-term valuation driver. For now, the key question is whether GEM-AKI can be launched, funded and eventually read out in a way that validates Gemini’s mechanism in a high-need hospital indication.
| Program | Indication | Status | Key endpoint / focus |
|---|---|---|---|
| GEM-AKI | Acute kidney injury | Planned Phase 2/3 | Death and/or need for dialysis |
| GEM-CKD | Chronic kidney disease | Completed Phase 1b PRIME | Safety, tolerability and inflammatory biomarkers |
| GEM-PSI | Post-surgical / hospital-acquired infection | Preclinical / development | Reduction of infection duration and severity |
| GEM-PBI | Severe burn infection prevention | Early development | Innate immune protection in vulnerable hospitalized patients |
4. Clinical Data: Key Results
Phase 1 in Healthy Volunteers
The first-in-human Phase 1 study of Gemini met its primary safety and tolerability endpoint. Revelation reported statistically significant dose-dependent changes across multiple pharmacodynamic biomarkers. These included significant mobilization of neutrophils and monocytes at medium and high doses, significant increases in NGAL at medium and high doses, and upregulation of IL-1RA, an anti-inflammatory mediator.
The safety-relevant point is that Revelation reported no significant increase in TNF-α at the highest dose and no significant increase in IL-1β in the cited analysis. For a TLR4 agonist, this is a key part of the story. TLR4 is involved in inflammatory activation, and uncontrolled activation could be dangerous. The company’s thesis is that Gemini can generate beneficial innate immune priming without triggering the kind of pro-inflammatory cytokine response associated with severe toxicity.
These Phase 1 data do not prove efficacy, but they support the idea that Gemini has measurable biological activity in humans and that its activity is not simply theoretical or limited to preclinical models. They also provide the first layer of safety support for testing in more clinically relevant patient populations.
Phase 1b PRIME in CKD Patients
PRIME is the most important clinical dataset reported by Revelation so far because it tested Gemini in patients with stage 3 and stage 4 chronic kidney disease. According to the company, Gemini significantly reduced cellular inflammation across key cytokines, including IL-1β, TNF-α, IL-6, IL-10 and IL-1RA. Revelation also reported restoration of normal cellular response to LPS stimulation, with statistically significant changes in IL-1β and TNF-α response.
The durability of the effect is especially relevant. Revelation reported effects lasting through 7 days after a single dose. If this pattern can be confirmed and translated into clinical benefit, it would support the idea that Gemini is not merely producing a transient laboratory signal but may be resetting aspects of innate immune function for a clinically useful window.
The correct interpretation remains balanced. PRIME provides encouraging biomarker and immunologic evidence, but it is not a pivotal outcomes trial. The central market question is whether the same immune rebalancing can reduce death and/or dialysis in AKI patients. Until that is demonstrated, Gemini remains promising but unproven.
Positive read-through: Gemini has shown coherent pharmacodynamic signals in early clinical settings, including real CKD patients. This makes the biological thesis more concrete than a purely preclinical hypothesis.
Prudent read-through: biomarkers and immune readouts are not the same as hard clinical outcomes. In AKI, many promising therapies have failed when tested against clinically meaningful endpoints.
5. Financial Analysis
5.1 Current Financial Position
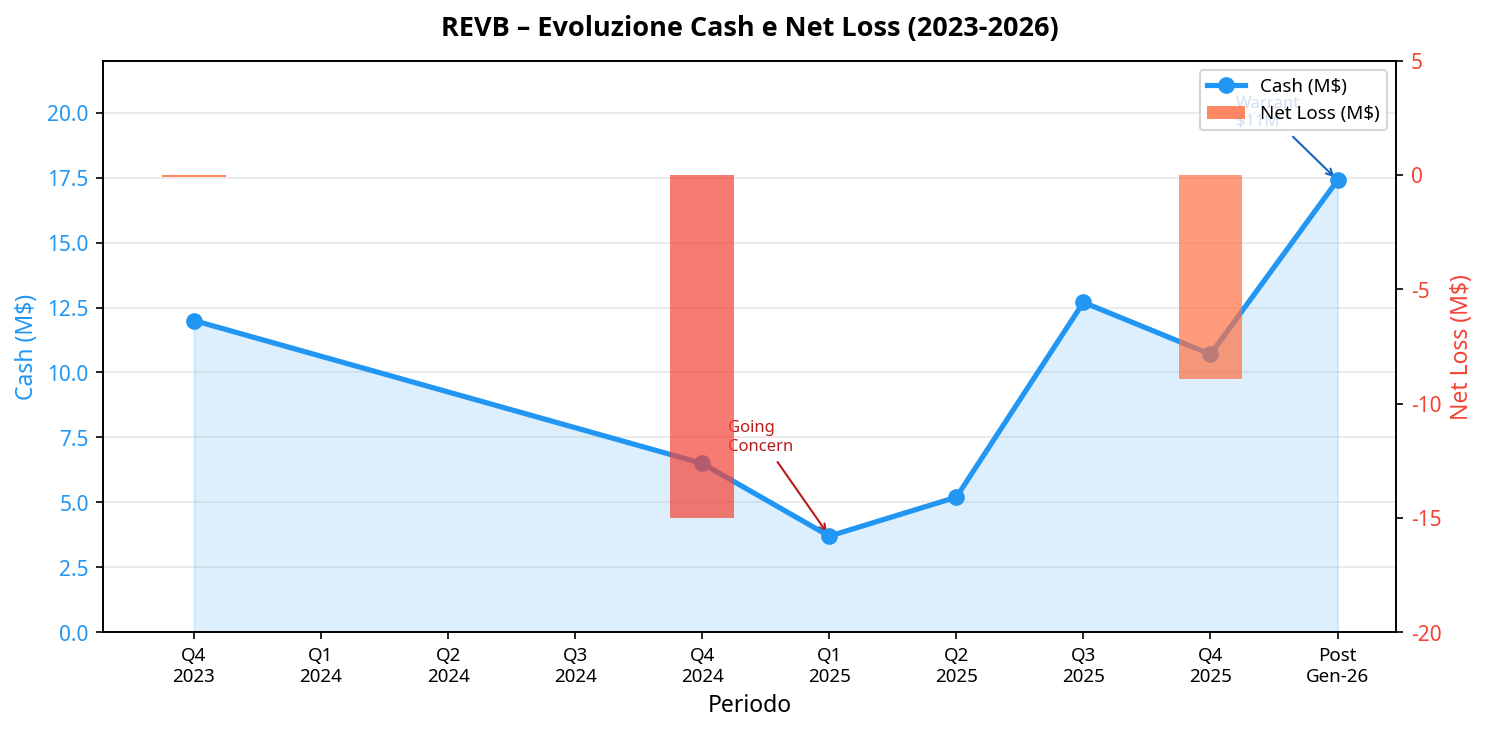
As of December 31, 2025, Revelation reported approximately $10.7 million in cash and cash equivalents. In January 2026, the company announced warrant exercises for approximately $11 million in gross proceeds, with approximately $6.7 million in net proceeds to the company. Management indicated that available cash, including those net proceeds, should fund operations into the first quarter of 2027.
That runway is useful but not sufficient to eliminate financing risk. A randomized, double-blind, placebo-controlled adaptive Phase 2/3 AKI trial of roughly 300 patients will require meaningful capital, clinical organization and execution discipline. Even if the trial design is efficient, it is still a hospital-based program in a critically ill population.
| Financial metric | Value / interpretation |
|---|---|
| Cash & equivalents at 12/31/2025 | Approximately $10.7M |
| Total debt reported by StockAnalysis | Approximately $0.75M |
| Net cash reported by StockAnalysis | Approximately $10.0M, or about $2.69 per share in that dataset |
| Stockholders’ equity | Approximately $8.86M |
| Book value per share | Approximately $5.59 in the referenced dataset |
| Working capital | Approximately $8.81M |
| Current ratio | 5.41 in the StockAnalysis dataset |
| Debt / equity | 0.08 in the StockAnalysis dataset |
5.2 Income Statement and Cash Burn
Revelation does not generate product revenue. The company reported a 2025 net loss of approximately $8.9 million, or a deeply negative EPS figure reflecting its small and changing share count. Cash used in operating activities in 2025 was approximately $8.3 million, compared with approximately $18.3 million in 2024. The improvement reflects a leaner cost profile and the absence of certain non-recurring legal-related payments that affected the prior year.
This lower burn rate is one of the more constructive financial points in the REVB story. A small team and lower overhead can extend runway. But the same lean structure becomes a limitation when the company attempts to run a more complex Phase 2/3 clinical program. The burn rate is likely to rise as the AKI trial moves from preparation to activation and enrollment.
| Year | Net loss | Operating cash used | Year-end cash |
|---|---|---|---|
| 2023 | Not representative due to non-recurring elements | Approximately -$7.3M | Approximately $12.0M |
| 2024 | Approximately -$15.0M | Approximately -$18.3M | Approximately $6.5M |
| 2025 | Approximately -$8.9M | Approximately -$8.3M | Approximately $10.7M |
5.3 Financing History
Revelation has relied on multiple financings to support operations. This is normal for a clinical-stage biotech, but the impact on existing shareholders has been severe because the company’s market value has been very small and the share price has been under pressure.
The recent financing history includes equity offerings, warrant structures and warrant exercises. In February 2024, the company announced a public offering of approximately $6.2 million. In May 2025, it announced a public offering of approximately $4 million involving shares and warrants. In July 2025, it announced another public offering of approximately $5 million. In January 2026, it announced the exercise of warrants for approximately $11 million in gross proceeds and approximately $6.7 million in net proceeds.
The shelf registration capacity cited in the research adds another layer to the dilution discussion. Having an active shelf can be useful because it gives the company flexibility to raise capital. For existing shareholders, however, it also represents potential future dilution, especially if capital is raised at depressed share prices.
The cleanest way for Revelation to improve the financial narrative would be to secure a partnership, grant, non-dilutive funding or less dilutive strategic financing tied to GEM-AKI. Without that, the equity market will continue to price the probability of additional share issuance.
6. Stock Analysis and Share Structure
6.1 Market Data as of April 30, 2026
REVB remains an extreme micro-cap. Public datasets showed slightly different values depending on timing, share count updates and whether recent warrant-related changes were reflected. StockAnalysis reported a market cap near $4.35 million, negative enterprise value near -$5.70 million, 3.72 million shares outstanding and a float near 3.27 million in its April 24, 2026 snapshot. Market data available on April 30 showed a price around $1.15 and a lower market cap near $3.04 million. The difference should be treated as a data timing issue, not a change in the core thesis.
Data verification note: for micro-caps with recent reverse splits, warrant exercises and changing share counts, market cap, float, short interest and cash per share can differ materially across providers. The latest SEC filing and company disclosures should be checked before each future update.
| Metric | Indicative value / comment |
|---|---|
| Price | Around $1.15 in the April 30, 2026 check |
| Market cap | Approximately $3.0M-$4.4M depending on provider and share count |
| Enterprise value | Negative in the StockAnalysis dataset |
| Shares outstanding | 3.72M in the StockAnalysis April 24 dataset |
| Float | 3.27M in the StockAnalysis dataset |
| 52-week range | Approximately $0.99-$40.08 in the referenced dataset |
| 52-week performance | Down more than 96% in the StockAnalysis dataset |
| 50-day / 200-day moving average | Approximately $1.25 / $4.90 in the StockAnalysis April dataset |
| Short interest | Provider-dependent; low as a percentage of shares outstanding in the referenced datasets |
| Insider ownership | Approximately 4.94% in the StockAnalysis dataset |
| Institutional ownership | Approximately 5.35% in the StockAnalysis dataset |
| P/B ratio | Approximately 0.21 in the StockAnalysis dataset |
The most striking data point is negative enterprise value. In simple terms, the market is valuing the company below estimated net cash. This can look attractive for speculative traders, but in a clinical-stage biotech it is not automatically bullish. It often means the market is discounting future cash burn, financing needs, going concern pressure and potential dilution.
For REVB, the negative enterprise value is less a clean valuation anomaly and more a signal of distrust. The market appears to be saying that the pipeline may have value, but that the path to realizing that value requires capital the company does not yet have on non-dilutive terms.
6.2 Reverse Stock Split History
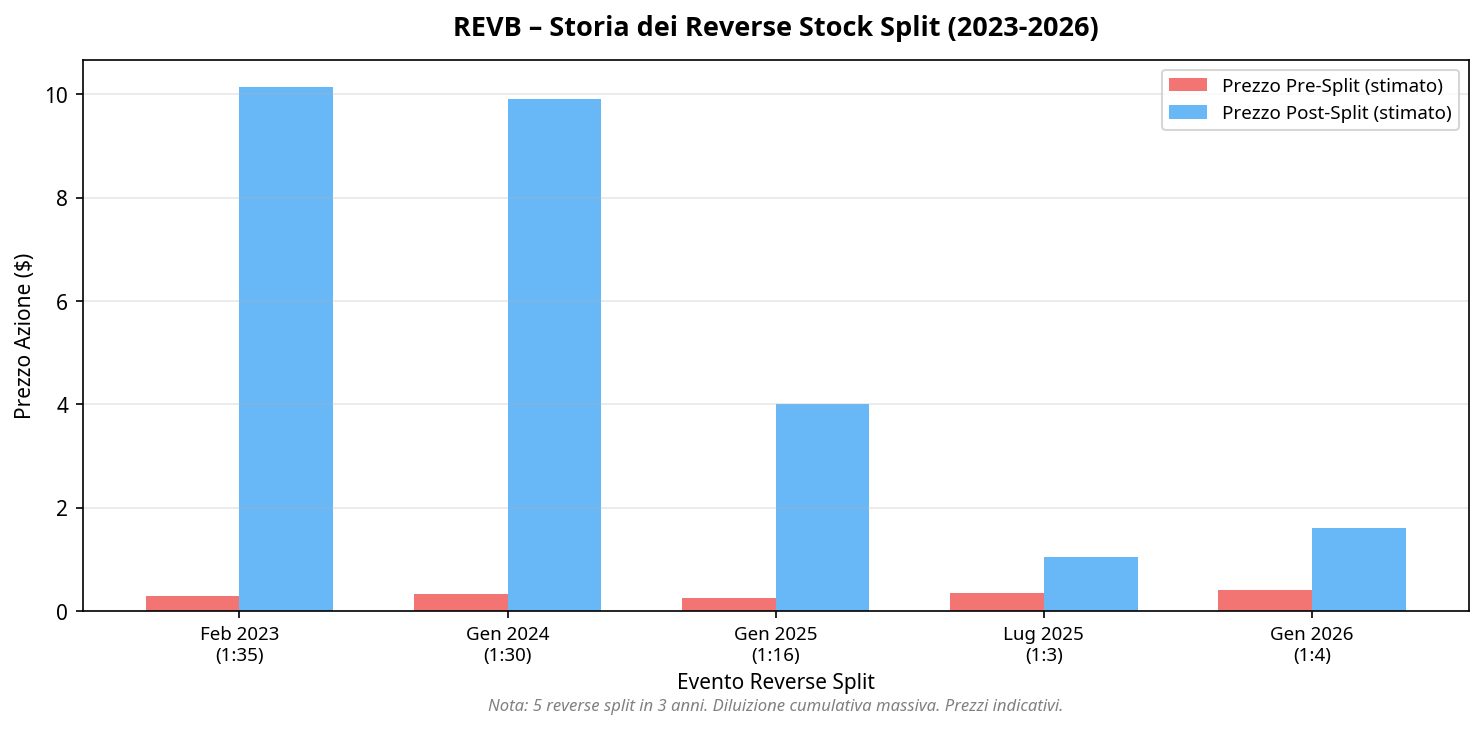
The most concerning equity-market feature is the repeated reverse stock split history. A reverse split does not destroy value by itself, but when it occurs repeatedly alongside capital raises, warrant issuance and a declining share price, it becomes the visible marker of a dilution cycle.
| Date | Ratio | Main reason / interpretation |
|---|---|---|
| February 2023 | 1-for-35 | NASDAQ compliance |
| January 2024 | 1-for-30 | NASDAQ compliance |
| January 2025 | 1-for-16 | NASDAQ compliance |
| July 2025 | 1-for-3 | NASDAQ compliance |
| January 2026 | 1-for-4 | NASDAQ compliance |
This sequence is a structural red flag. It does not mean a speculative rally is impossible. Micro-cap biotech stocks with small floats and real catalysts can move sharply. But it does mean the long-term shareholder base has been heavily damaged, and new investors must understand that future financing could continue to pressure the equity.
7. Addressable Market and Commercial Opportunity
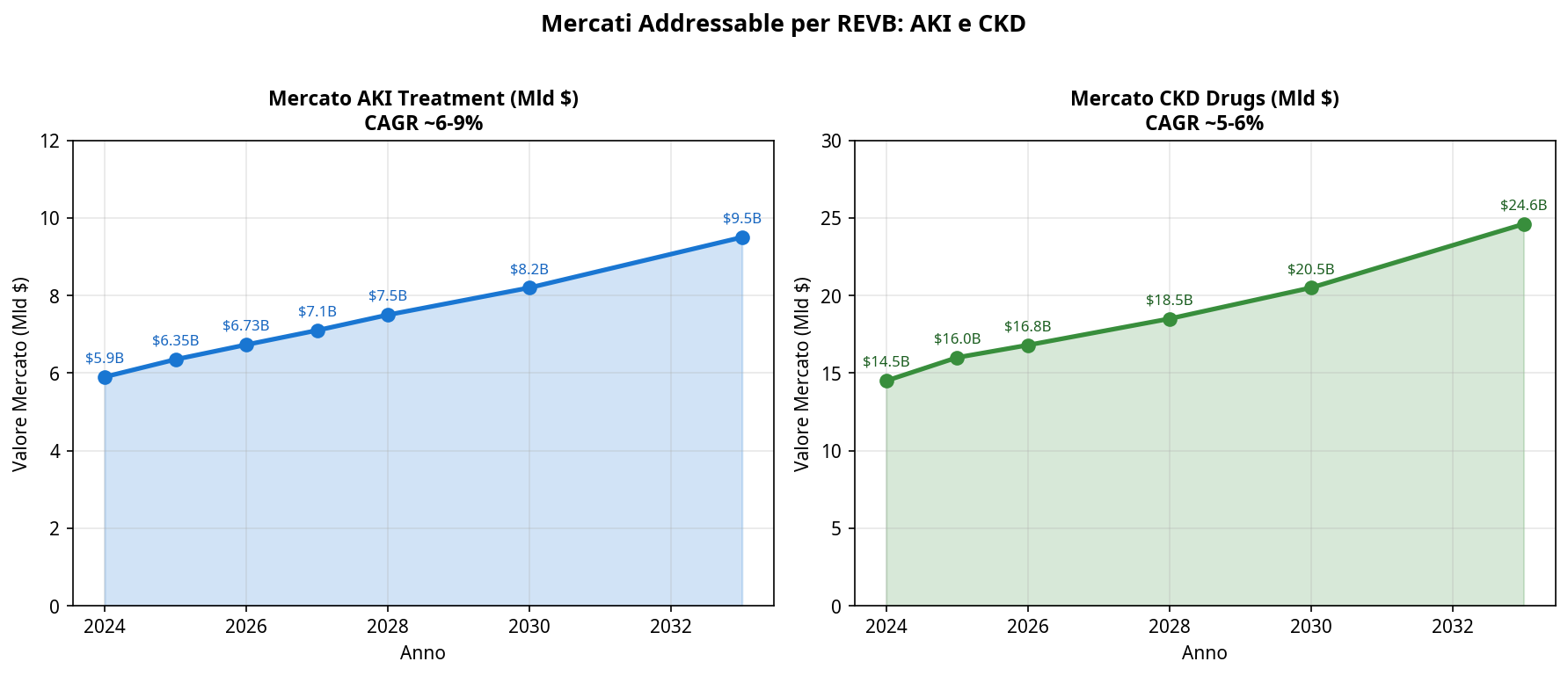
7.1 Acute Kidney Injury
AKI is one of the most important unmet needs in hospital medicine. It is common in hospitalized patients, more common in intensive care, and associated with mortality, dialysis, longer ICU stays, higher cost of care and progression toward chronic kidney disease. Revelation estimates roughly 6.8 million hospitalized AKI patients per year in the United States by applying an estimated 20% AKI incidence to approximately 34 million annual hospitalizations.
The company and third-party market sources point to a large potential commercial opportunity. Global AKI treatment market estimates vary by source, methodology and definition, but several industry datasets place the market in the multi-billion-dollar range, with expected growth through the end of the decade. For a company the size of Revelation, even a narrow slice of a clinically validated AKI market would be meaningful.
The commercial attraction is therefore obvious. A therapy that can reduce death and/or dialysis in a defined AKI population could become clinically and economically relevant. It could reduce ICU burden, dialysis use, complications and long-term progression to chronic kidney disease. The challenge is equally obvious: AKI has been a graveyard for many promising therapies because the condition is heterogeneous, acute, complex and influenced by many comorbidities and hospital variables.
7.2 Chronic Kidney Disease
CKD is an even larger chronic disease population, with tens of millions of patients in the United States alone. The global CKD drug market is also multi-billion-dollar and growing, driven by aging populations, diabetes, hypertension, cardiovascular disease and improved diagnosis.
For Revelation, the near-term importance of CKD is not mainly commercial. It is scientific. PRIME provides patient-level biological evidence in a kidney disease population and supports the rationale for testing Gemini in AKI. In the future, GEM-CKD could become its own development path, but in the current market setup CKD functions primarily as proof-of-biology supporting the higher-impact AKI program.
8. Competitive Landscape
The AKI competitive landscape includes more than 30 companies and programs according to third-party pipeline summaries, but the majority face the same core problem: translating plausible biological mechanisms into clear clinical benefit in a difficult acute-care setting. Complement inhibition, alkaline phosphatase replacement, protective peptides, metabolic modulation and anti-inflammatory strategies have all been explored.
| Company | Drug / program | Indicative phase | Mechanism / focus |
|---|---|---|---|
| AstraZeneca / Alexion | Ravulizumab | AKI competitive landscape / Phase 3 context | C5 complement inhibition |
| AM-Pharma / Kyowa Kirin | Ilofotase alfa | Phase 3 historical AKI landscape | Recombinant alkaline phosphatase |
| Novartis | TIN816 | Phase 2b context | Renal / inflammatory approach |
| Guard Therapeutics | RMC-035 | Phase 2 | Protective peptide |
| Arch Biopartners | LSALT peptide | Phase 1b/2 | Anti-inflammatory peptide |
| Kelifarma | KELI-101 | Phase 1b/2 context | Kidney injury / inflammatory program |
| Revelation Biosciences | Gemini / GEM-AKI | Planned Phase 2/3 | TLR4 agonist / trained immunity / innate immune rebalancing |
Gemini’s differentiating claim is that it does not merely block a single downstream inflammatory pathway. Instead, it aims to rebalance innate immunity upstream. This could be an advantage if the biology translates into broad protection across heterogeneous AKI patients. It could also be a weakness if the mechanism is too indirect, too variable across patient populations or insufficient to move hard clinical endpoints.
Competition from larger companies is an important risk. Companies such as AstraZeneca, Novartis or other well-capitalized sponsors have greater clinical, regulatory and financial capacity. If a larger player produces strong data first, Gemini’s market opportunity could narrow. Conversely, persistent failure by larger competitors would keep the unmet need open and could make a differentiated mechanism like Gemini more interesting if Revelation can execute.
9. SWOT Analysis
Strengths
Differentiated mechanism of action. Gemini/PHAD is built around innate immune rebalancing and trained immunity, not classic broad immunosuppression.
FDA-aligned development pathway. The January 2026 agreement on a single adaptive Phase 2/3 trial creates a potentially efficient route toward NDA submission if the data are positive.
Multi-indication platform. The same candidate is being explored in AKI, CKD, post-surgical infection and severe burn infection prevention, creating several potential value paths from one scientific platform.
Encouraging PRIME data. The CKD biomarker results and investigator commentary support the biological rationale and give the story more substance than a purely preclinical hypothesis.
Weaknesses
Extremely small market capitalization. A company valued at only a few million dollars must finance a complex clinical trial that could require far more capital than its current equity value.
Severe dilution history. Repeated capital raises, warrant structures and reverse stock splits have damaged the equity story.
Going concern pressure. Runway into Q1 2027 does not eliminate the need for additional financing.
Small internal team. The company’s ability to run a complex trial depends heavily on external execution through CROs and advisors.
Opportunities
Large unmet need in AKI. A therapy that reduces death and/or dialysis could be clinically valuable and commercially meaningful.
Partnership or licensing potential. Stronger clinical progress could attract interest from larger pharmaceutical or biotech companies.
Negative enterprise value setup. The depressed valuation may attract speculative traders looking for asymmetric biotech setups.
Pipeline expansion. GEM-PSI and GEM-PBI add long-term optionality if the platform is validated.
Threats
Clinical failure risk. AKI is historically difficult, and early biomarker activity may not translate into clinical endpoints.
Competition from larger companies. Better-funded sponsors have stronger development and commercial resources.
NASDAQ compliance and delisting risk. The reverse split history shows that listing compliance has been a recurring issue.
Future financing risk. Additional capital raises could be highly dilutive if done at depressed share prices.
10. Valuation and Analyst Targets
Analyst coverage of REVB is very limited, which is consistent with the company’s micro-cap status. Available targets vary widely and should be read with caution. Some third-party platforms show high theoretical price targets, but those targets are often based on very small analyst samples or issuer-compensated research. Zacks SCR, for example, discloses compensation from the issuer for coverage, which reduces the independence value of the rating and target.
| Source / dataset | Rating / target context | Important caveat |
|---|---|---|
| Zacks SCR | High target price in January 2026 research | Issuer-compensated research; should be treated with caution |
| TradingView consensus | Very limited analyst sample | Consensus is not robust with only one or very few analysts |
| Investing.com / aggregators | Wide target range | Must be checked against updated share count and filings |
| Quantitative / technical models | Often negative | Reflect weak price momentum and dilution history |
A conservative approach is to look at net cash per share, but this metric is not a simple floor. In a clinical-stage biotech, cash is consumed by operating burn and clinical development. It can also be offset by future warrants, new equity issuance, payables and trial obligations. Trading below estimated cash per share may indicate undervaluation, but it may also indicate that the market expects the cash to be spent and shareholders to be diluted before the pipeline creates value.
The more useful valuation framework for REVB is scenario-based. In a successful GEM-AKI scenario, the current market capitalization would likely appear far too low relative to the potential opportunity. In a delayed or dilutive scenario, the current low valuation may be justified or even still too high. This is why the stock should be analyzed as a clinical and financing catalyst story rather than a traditional multiple-based investment.
11. Catalysts and Risks
Positive Catalysts to Watch
2026 is a crucial year for Revelation. The most important potential catalyst is the formal initiation of the GEM-AKI Phase 2/3 trial. The market will need to see practical confirmation, not just broad language: CRO selection, clinical site activation, enrollment expectations, dosing plan, drug supply readiness, regulatory clarity and cash planning.
Additional catalysts include further PRIME data presentations at scientific conferences, management updates on trial infrastructure, potential partnerships or licensing discussions, quarterly results and any new financing structure that reduces dilution concerns. Earnings are not important because of revenue, since the company has none. They are important because they update cash balance, burn rate, runway and the operational timeline.
Main Risks
The clinical risk is the largest. AKI is a difficult development area. Patients are heterogeneous, the disease course is acute, standard of care varies across settings and endpoints such as death and dialysis are hard to move. Positive Phase 1 or Phase 1b biomarkers are encouraging, but they do not guarantee clinical efficacy.
The financial risk is equally critical. The company will likely need significant additional capital to complete the planned Phase 2/3 trial. If capital is raised through equity or warrant-heavy structures at depressed prices, dilution could remain severe.
The regulatory risk is that FDA requirements could evolve. Agreement on a pathway is positive, but it does not guarantee that the trial will succeed, that the data will be sufficient, or that the FDA will not require additional analyses, safety information or confirmatory evidence.
The competitive risk is that a larger company could achieve positive AKI data or approval first, reducing Gemini’s perceived opportunity. Even if Gemini works, commercial positioning will depend on label, population, timing, hospital adoption, pricing and comparative evidence.
The NASDAQ/listing risk remains relevant because the company’s share price has repeatedly fallen into compliance pressure. Repeated reverse splits can keep a listing alive temporarily, but they also damage investor confidence and often reinforce the perception of a structurally weak equity.
12. Bull, Base and Bear Scenarios
| Scenario | What needs to happen | Editorial implication |
|---|---|---|
| Bull case | Clear GEM-AKI initiation, credible CRO/site plan, manageable funding, no immediate punitive dilution, continued scientific support for PRIME, possible partnership or strategic interest. | REVB could become a highly speculative but credible AKI micro-cap story with meaningful repricing potential. |
| Base case | The company continues trial preparation, burns cash slowly, raises additional capital on dilutive terms, survives toward the next clinical updates but does not fully solve the financing overhang. | The stock remains volatile, with rallies on news and structural pressure between catalysts. |
| Bear case | Trial delays, punitive capital raise, further share weakness, renewed NASDAQ pressure, disappointing clinical/regulatory updates or inability to fund the AKI program. | The risk of additional value destruction, dilution and reverse split pressure remains high. |
13. Bottom Line
Revelation Biosciences is a high-risk, high-optional-value biotech case. On one side, the company has built a scientific story that is more substantial than many micro-cap biotech narratives: Gemini has a differentiated mechanism, early clinical data support pharmacodynamic activity, the FDA-aligned AKI pathway is potentially efficient, and the Advisory Board adds clinical credibility to the planned Phase 2/3 program.
On the other side, the structural risks are severe. The market capitalization is extremely small, the reverse split history is difficult, the company has no revenue, the going concern language and runway limitations matter, and significant additional funding will likely be needed to complete the pivotal AKI program. The negative enterprise value reflects not only potential undervaluation, but also deep market skepticism toward the company’s ability to turn the pipeline into value without further dilution.
For speculative biotech traders, REVB can belong on the radar as a catalyst-driven micro-cap with an unusually clear AKI development concept. For conservative investors, the risk profile remains incompatible with a prudent investment framework. The decisive variables over the next several months are straightforward: financing, formal GEM-AKI trial initiation, enrollment visibility, and the quality of future clinical/regulatory updates.
Disclaimer: This content is provided for informational and educational purposes only and does not constitute financial, investment, legal, tax, medical or trading advice. It is not a recommendation to buy, sell or hold any security. Clinical-stage biotechnology companies involve high risk, including clinical failure, regulatory delays, dilution, delisting risk and possible loss of the entire capital invested. Readers should conduct their own due diligence and consult qualified professionals before making financial decisions.
Prossimo catalyst da monitorare: il catalyst operativo più importante è l’avvio formale e il percorso di esecuzione dello studio adattivo Phase 2/3 GEM-AKI. Revelation ha indicato di stare costruendo nel 2026 l’infrastruttura necessaria, inclusi CRO, advisory input e clinical drug supply, dopo l’accordo con la FDA sul disegno adattivo per AKI.
Società
Biotech clinical-stage
Asset principale
Gemini / PHAD®
Target core
TLR4 / immunità innata
Rischio chiave
Diluizione + execution
Sommario Esecutivo
Revelation Biosciences, Inc. (NASDAQ: REVB) è una società biofarmaceutica in stadio clinico con sede a San Diego, California, focalizzata sullo sviluppo di terapie innovative basate sulla modulazione del sistema immunitario innato. Il suo prodotto principale, Gemini, è una formulazione endovenosa proprietaria di PHAD® (phosphorylated hexaacyl disaccharide), un agonista del recettore Toll-like 4 progettato per “riprogrammare” o ribilanciare la risposta infiammatoria innata, con l’obiettivo di prevenire o ridurre il danno d’organo associato a infiammazione acuta e cronica.
Il 2025 e l’inizio del 2026 hanno rappresentato un periodo di svolta per la società. Revelation ha riportato il completamento positivo dello studio PRIME Phase 1b in pazienti con chronic kidney disease, ha raggiunto un accordo importante con la FDA sul percorso di approvazione proposto per Gemini nell’acute kidney injury, e ha formato un Advisory Board internazionale di alto profilo per il trial adattivo Phase 2/3 pianificato. Questi sviluppi hanno spostato Gemini da una storia iniziale basata su biomarker verso un percorso clinico-regolatorio più definito in un’indicazione con forte bisogno medico insoddisfatto.
Allo stesso tempo, REVB rimane una storia azionaria ad altissimo rischio. La capitalizzazione di mercato è estremamente ridotta, il titolo ha perso quasi tutto il proprio valore nell’ultimo anno e la società ha completato ripetuti reverse stock split negli ultimi tre anni per mantenere la compliance con i requisiti NASDAQ. La struttura finanziaria è fragile, il bisogno di capitale aggiuntivo resta materiale e il trial AKI pianificato richiederà una capacità esecutiva molto superiore rispetto ai precedenti lavori Phase 1 e Phase 1b.
La lettura più importante è che Revelation non è una semplice “cash box” sottovalutata e non è una biotech convenzionalmente de-risked. È una micro-cap clinical-stage speculativa con una piattaforma di immunomodulazione differenziata, dati biomarker iniziali promettenti, un percorso AKI potenzialmente efficiente e allineato con FDA, ma anche con severi rischi di finanziamento e diluizione. Il bull case dipende dalla capacità della biologia di Gemini di tradursi in endpoint clinici duri, come riduzione di morte e/o dialisi. Il bear case dipende dal pattern più comune delle micro-cap biotech: diluizione, ritardi, attrito regolatorio, debole fiducia del mercato e nuova pressione sul capitale.
1. Profilo Aziendale
Revelation Biosciences è stata incorporata nel 2019 come Petra Acquisition, Inc. e ha assunto la denominazione attuale nel gennaio 2022 a seguito di una fusione SPAC. La società opera con una struttura estremamente snella e con un modello di business tipico di una biotech in stadio clinico: nessun prodotto approvato, nessun ricavo operativo e dipendenza totale da finanziamenti esterni per sostenere ricerca, sviluppo, attività regolatorie e operazioni corporate.
La società è guidata da James M. Rolke, cofondatore, Chief Executive Officer e Chairman, con lunga esperienza nel settore biotecnologico. Chester Stanley Zygmont III ricopre il ruolo di Chief Financial Officer e Corporate Secretary. La base interna di dipendenti è molto ridotta: questo aiuta a mantenere il burn rate più contenuto rispetto a un’organizzazione clinica più ampia, ma significa anche che la società deve fare forte affidamento su CRO, consulenti esterni, advisor scientifici, specialisti regolatori, siti clinici e collaboratori accademici per portare avanti programmi complessi.
La tecnologia core della società è stata sviluppata anche attraverso la collaborazione con Vanderbilt University. Nell’ottobre 2022, Revelation ha stipulato con Vanderbilt un accordo di licenza esclusiva mondiale per applicazioni infettive di PHAD. Questo accordo sostiene la narrativa multi-indicazione intorno a Gemini e crea un ponte scientifico verso infezioni post-chirurgiche, infezioni ospedaliere, infezioni post-ustione e altri contesti in cui disregolazione immunitaria e risposta innata possono influenzare gli outcome clinici.
Dal punto di vista del mercato azionario, questo profilo crea un trade-off familiare ma molto marcato. Revelation è abbastanza piccola perché qualsiasi validazione clinica o strategica credibile possa incidere in modo sproporzionato sulla valutazione. Ma è anche abbastanza piccola perché formazione di capitale, compliance di quotazione e capacità esecutiva restino problemi costanti. Una società con team ridotto e senza ricavi non può assorbire setback clinici o condizioni di finanziamento deboli come uno sponsor biotech o farmaceutico più grande.
| Caratteristica | Dettaglio |
|---|---|
| Sede | San Diego, California |
| Storia corporate | Incorporata nel 2019 come Petra Acquisition, Inc.; rinominata Revelation Biosciences nel gennaio 2022 |
| Dipendenti | Struttura molto snella; StockAnalysis riporta 9 dipendenti |
| CEO | James M. Rolke, cofondatore, CEO e Chairman |
| CFO | Chester Stanley Zygmont III |
| Settore | Biotecnologia / Healthcare |
| Prodotto principale | Gemini, formulazione proprietaria di PHAD® |
| Licenza chiave | Vanderbilt University, ottobre 2022, per applicazioni infettive di PHAD |
2. Tecnologia Core: Gemini e Meccanismo d’Azione
Il cuore della strategia di Revelation è Gemini, una formulazione endovenosa proprietaria di PHAD® (phosphorylated hexaacyl disaccharide). PHAD è un agonista sintetico del recettore Toll-like 4, un recettore chiave dell’immunità innata coinvolto nel riconoscimento di segnali di pericolo associati a patogeni, danno tissutale e stress biologico.
Il meccanismo si basa sul concetto di trained immunity, o immunità addestrata. La tesi di Revelation è che una stimolazione controllata di TLR4 con Gemini possa ribilanciare le cellule dell’immunità innata, soprattutto monociti e neutrofili, spostandole da uno stato infiammatorio patologico o di immunoparalisi verso una risposta più protettiva e controllata. Questo è diverso dall’immunosoppressione classica. Invece di bloccare semplicemente l’attività immunitaria, Gemini punta a normalizzare e migliorare la qualità della risposta immunitaria a stress successivi come ischemia, infezione o trauma.
Questo è il motivo scientifico principale per cui Gemini viene esplorato in più indicazioni. AKI, CKD, infezioni post-chirurgiche e prevenzione delle infezioni in ustioni gravi sono setting clinici diversi, ma condividono un tema comune: disfunzione infiammatoria, attivazione dell’immunità innata o immunoparalisi possono influenzare danno d’organo, rischio infettivo e recupero. Se Gemini riuscisse a ribilanciare in modo sicuro questo sistema, lo stesso candidato potrebbe avere optionalità di piattaforma.
Un aspetto importante di sicurezza nei dati clinici iniziali è la selettività della risposta. Secondo Revelation, Gemini non ha prodotto aumenti significativi di TNF-α alla dose più alta testata e non ha prodotto aumenti significativi di IL-1β nell’analisi Phase 1 citata, mostrando invece upregolazione di mediatori protettivi o anti-infiammatori come IL-1RA, NGAL e IL-10. Per un agonista TLR4, questa distinzione è centrale perché un’attivazione non controllata di TLR4 potrebbe teoricamente produrre tossicità infiammatoria eccessiva.
“The activity observed with a single dose of Gemini in patients is shocking. This effect suggests a meaningful step forward in addressing the underlying immune dysregulation observed in patients with chronic kidney disease.”Dr. Adam Horeish, MD, Principal Investigator, Balboa Research, citato da Revelation Biosciences
La domanda irrisolta non è se Gemini abbia un meccanismo plausibile. La domanda irrisolta è se l’attività sui biomarker e il ribilanciamento immunitario possano tradursi in outcome clinici significativi in AKI: meno morti, meno dialisi, migliore recupero renale e migliori outcome ospedalieri. È questo il ponte che il trial Phase 2/3 pianificato dovrà provare a costruire.
3. Pipeline Clinica

La pipeline di Revelation è costruita interamente intorno a Gemini e applica lo stesso concetto di ribilanciamento dell’immunità innata a quattro aree terapeutiche. Questa concentrazione dà coerenza scientifica alla storia, ma concentra anche il rischio. Se il meccanismo di Gemini non produrrà risultati clinicamente rilevanti in AKI o CKD, la narrativa di piattaforma si indebolirebbe rapidamente. Al contrario, se il programma AKI produrrà evidenza clinica credibile, la stessa piattaforma potrebbe acquisire valore anche nelle indicazioni aggiuntive.
3.1 GEM-AKI — Danno Renale Acuto
GEM-AKI è il programma più avanzato e più importante della società. L’acute kidney injury è caratterizzato da una rapida perdita della funzione renale. Colpisce una quota importante dei pazienti ospedalizzati e più della metà dei pazienti in terapia intensiva secondo l’epidemiologia citata dalla società e da fonti terze. L’AKI severo può richiedere dialisi, aumentare la mortalità, prolungare la permanenza in ICU e contribuire alla progressione verso chronic kidney disease o end-stage renal disease.
Negli Stati Uniti, Revelation stima circa 6,8 milioni di pazienti AKI ospedalizzati ogni anno applicando una stima del 20% di incidenza AKI a circa 34 milioni di ricoveri annui. La società cita anche un costo significativo per Medicare e conseguenze cliniche severe, soprattutto nei pazienti che richiedono dialisi. Il punto commerciale più importante è che non esiste ancora una terapia farmacologica ampia approvata specificamente per trattare l’AKI nella popolazione ospedaliera generale, con terlipressina come eccezione specifica nel subset HRS-AKI.
Il 21 gennaio 2026, Revelation ha annunciato di aver raggiunto un accordo con la FDA sul percorso di approvazione proposto per Gemini in AKI. Due elementi sono centrali. Primo, l’endpoint primario allineato con FDA è un composito clinicamente rilevante di morte e/o necessità di dialisi. Secondo, Revelation ha dichiarato che dati positivi da un singolo studio adattivo Phase 2/3 di circa 300 pazienti potrebbero essere sufficienti per supportare la presentazione di una New Drug Application.
Il disegno pianificato è diviso in due parti. La Parte 1 valuterà diversi regimi di dosaggio rispetto al placebo. La Parte 2 procederà come porzione Phase 3 utilizzando il regime di dosaggio più sicuro identificato nella Parte 1. I dati di entrambe le parti potranno essere inclusi nelle analisi degli endpoint primari e secondari. Questo è potenzialmente importante perché può comprimere il percorso di sviluppo clinico ed evitare una Phase 2 totalmente separata seguita da una Phase 3 totalmente separata. Per una micro-cap, questa efficienza conta.
Il limite è che anche un trial adattivo Phase 2/3 relativamente efficiente non è né economico né semplice. I pazienti AKI sono clinicamente complessi, i trial ospedalieri richiedono forte execution dei siti e la cattura degli endpoint deve essere rigorosa. Revelation avrà bisogno di infrastruttura clinica, performance della CRO, drug supply, attivazione dei siti, disciplina nell’arruolamento, monitoraggio sicurezza e capitale sufficiente per mantenere il programma in movimento.
Il 6 aprile 2026, Revelation ha annunciato la formazione di un AKI Advisory Board con specialisti in nefrologia e terapia intensiva da istituzioni come Emory University, University of Alberta, University of Cincinnati/Cincinnati Children’s, UAB e University of Münster. Questo non de-riska il trial da solo, ma supporta qualità del protocollo, rilevanza clinica e pianificazione dell’execution.
3.2 GEM-CKD — Chronic Kidney Disease e PRIME
GEM-CKD ha completato lo studio Phase 1b PRIME in pazienti con chronic kidney disease stadio 3 e 4. La società ha riportato che lo studio ha raggiunto l’endpoint primario di sicurezza e tollerabilità. Revelation ha anche riportato che oltre l’85% dei pazienti aveva almeno una citochina elevata prima del trattamento e che oltre il 60% presentava IL-1β e IL-6 elevate al basale.
Secondo la società, Gemini ha ridotto significativamente il numero di citochine elevate a tutti i timepoint misurati fino a 7 giorni dopo una singola dose rispetto al placebo. Revelation ha anche riportato normalizzazione dell’infiammazione di fondo verso livelli osservati nei soggetti sani, ripristino della risposta cellulare alla stimolazione e correzione dell’immunoparalisi spesso osservata nella malattia cronica. Nei risultati PRIME citati non sono stati riportati eventi avversi seri, e gli eventi avversi alla dose target sono stati descritti come lievi.
I dati PRIME sono importanti perché creano continuità biologica tra il lavoro iniziale di sicurezza nei volontari sani e il concetto pivotale in AKI. La CKD non è AKI, e i risultati biomarker non equivalgono a outcome clinici da approvazione. Ma PRIME suggerisce che Gemini può produrre attività immunologica misurabile in una popolazione reale con malattia renale. È per questo che il mercato può trattare ulteriori presentazioni PRIME come catalyst di supporto anche se GEM-AKI resta il driver di valore principale.
3.3 GEM-PSI — Infezione Post-Chirurgica
GEM-PSI è sviluppato in collaborazione con Vanderbilt University come potenziale terapia per prevenzione o trattamento di infezioni batteriche acquisite in ospedale. L’opportunità prevista include infezioni post-chirurgiche, infezioni post-ustione e infezioni del tratto urinario. La base scientifica è che il pretrattamento sistemico con PHAD ha mostrato, in modelli preclinici citati da Revelation, riduzioni significative di durata e severità delle infezioni batteriche sia gram-positive sia gram-negative.
Questo programma è strategicamente utile perché espande Gemini oltre la malattia renale e rafforza la tesi di piattaforma sull’immunità innata. Commercialmente, però, resta secondario finché Revelation non dimostrerà che la modulazione immunitaria di Gemini può produrre outcome clinicamente significativi in un programma più avanzato.
3.4 GEM-PBI — Prevenzione Infezioni in Ustioni Gravi
GEM-PBI è stato annunciato nell’aprile 2025 ed è sviluppato per la prevenzione delle infezioni in pazienti con ustioni gravi che richiedono ospedalizzazione. Questa indicazione si inserisce nella logica della piattaforma: i pazienti con ustioni severe sono vulnerabili, la risposta immune può diventare disfunzionale, il rischio infettivo è elevato e potrebbe esistere un ruolo per priming o ribilanciamento controllato dell’immunità.
Come GEM-PSI, GEM-PBI è in fase più iniziale e va considerato optionality di lungo periodo più che driver di valutazione di breve termine. Per ora, la domanda chiave è se GEM-AKI potrà essere avviato, finanziato e letto in modo da validare il meccanismo di Gemini in un’indicazione ospedaliera ad alto bisogno.
| Programma | Indicazione | Stato | Endpoint / focus chiave |
|---|---|---|---|
| GEM-AKI | Danno renale acuto | Phase 2/3 pianificata | Morte e/o necessità di dialisi |
| GEM-CKD | Malattia renale cronica | Phase 1b PRIME completata | Sicurezza, tollerabilità e biomarker infiammatori |
| GEM-PSI | Infezione post-chirurgica / ospedaliera | Preclinico / sviluppo | Riduzione durata e severità infezione |
| GEM-PBI | Prevenzione infezioni in ustioni gravi | Sviluppo iniziale | Protezione immunitaria innata in pazienti ospedalizzati vulnerabili |
4. Dati Clinici: Risultati Chiave
Phase 1 in Volontari Sani
Lo studio Phase 1 first-in-human di Gemini ha raggiunto l’endpoint primario di sicurezza e tollerabilità. Revelation ha riportato cambiamenti dose-dipendenti statisticamente significativi in diversi biomarker farmacodinamici. Questi includevano mobilizzazione significativa di neutrofili e monociti alle dosi media e alta, aumento significativo di NGAL alle dosi media e alta, e upregolazione di IL-1RA, un mediatore anti-infiammatorio.
Il punto più rilevante per la sicurezza è che Revelation ha riportato assenza di aumento significativo di TNF-α alla dose più alta e assenza di aumento significativo di IL-1β nell’analisi citata. Per un agonista TLR4, questo è un elemento centrale. TLR4 è coinvolto nell’attivazione infiammatoria, e un’attivazione non controllata potrebbe essere pericolosa. La tesi della società è che Gemini possa generare un priming benefico dell’immunità innata senza innescare una risposta citochinica pro-infiammatoria associata a tossicità severa.
Questi dati Phase 1 non dimostrano efficacia, ma supportano l’idea che Gemini abbia attività biologica misurabile nell’uomo e che la sua attività non sia soltanto teorica o limitata a modelli preclinici. Forniscono inoltre il primo livello di supporto di sicurezza per il test in popolazioni di pazienti clinicamente più rilevanti.
Phase 1b PRIME in Pazienti CKD
PRIME è il dataset clinico più importante riportato finora da Revelation perché ha testato Gemini in pazienti con chronic kidney disease stadio 3 e 4. Secondo la società, Gemini ha ridotto significativamente l’infiammazione cellulare su citochine chiave, incluse IL-1β, TNF-α, IL-6, IL-10 e IL-1RA. Revelation ha anche riportato ripristino della normale risposta cellulare alla stimolazione con LPS, con cambiamenti statisticamente significativi nella risposta di IL-1β e TNF-α.
La durata dell’effetto è particolarmente rilevante. Revelation ha riportato effetti fino a 7 giorni dopo una singola dose. Se questo pattern sarà confermato e tradotto in beneficio clinico, sosterrà l’idea che Gemini non produca soltanto un segnale transitorio di laboratorio, ma possa resettare aspetti dell’immunità innata per una finestra clinicamente utile.
L’interpretazione corretta resta bilanciata. PRIME fornisce evidenza incoraggiante su biomarker e immunologia, ma non è uno studio pivotale su outcome. La domanda centrale per il mercato è se lo stesso ribilanciamento immunitario possa ridurre morte e/o dialisi nei pazienti AKI. Fino a quando questo non sarà dimostrato, Gemini rimane promettente ma non provato.
Lettura positiva: Gemini ha mostrato segnali farmacodinamici coerenti in contesti clinici iniziali, inclusi pazienti reali con CKD. Questo rende la tesi biologica più concreta rispetto a una pura ipotesi preclinica.
Lettura prudente: biomarker e readout immunitari non equivalgono a endpoint clinici duri. In AKI, molte terapie promettenti hanno fallito quando testate su endpoint clinicamente rilevanti.
5. Analisi Finanziaria

5.1 Posizione Finanziaria Attuale
Al 31 dicembre 2025, Revelation ha riportato circa $10,7 milioni in cash and cash equivalents. Nel gennaio 2026, la società ha annunciato esercizi di warrant per circa $11 milioni di proventi lordi, con circa $6,7 milioni netti per la società. Il management ha indicato che la cassa disponibile, inclusi quei proventi netti, dovrebbe finanziare le operazioni fino al primo trimestre 2027.
Questo runway è utile, ma non elimina il rischio finanziario. Uno studio AKI Phase 2/3 adattivo, randomizzato, double-blind, placebo-controlled, con circa 300 pazienti, richiederà capitale significativo, organizzazione clinica e disciplina esecutiva. Anche se il disegno del trial è efficiente, resta un programma ospedaliero in una popolazione criticamente malata.
| Metrica finanziaria | Valore / interpretazione |
|---|---|
| Cash & equivalents al 31/12/2025 | Circa $10.7M |
| Debito totale riportato da StockAnalysis | Circa $0.75M |
| Net cash riportata da StockAnalysis | Circa $10.0M, pari a circa $2.69 per share in quel dataset |
| Stockholders’ equity | Circa $8.86M |
| Book value per share | Circa $5.59 nel dataset citato |
| Working capital | Circa $8.81M |
| Current ratio | 5.41 nel dataset StockAnalysis |
| Debt / equity | 0.08 nel dataset StockAnalysis |
5.2 Conto Economico e Cash Burn
Revelation non genera ricavi da prodotto. La società ha riportato una perdita netta 2025 di circa $8,9 milioni, con EPS profondamente negativo anche per effetto del conteggio azionario ridotto e variabile. Il cash used in operating activities nel 2025 è stato circa $8,3 milioni, rispetto a circa $18,3 milioni nel 2024. Il miglioramento riflette una struttura dei costi più leggera e l’assenza di alcuni pagamenti legali non ricorrenti che avevano inciso sull’anno precedente.
Questo burn rate più basso è uno degli elementi finanziari più costruttivi della storia REVB. Un team piccolo e overhead contenuto possono estendere il runway. Ma la stessa struttura snella diventa un limite quando la società prova a eseguire un programma clinico Phase 2/3 più complesso. È probabile che il burn rate aumenti se il trial AKI passerà dalla preparazione all’attivazione e all’arruolamento.
| Anno | Net loss | Cash operativo usato | Cash fine anno |
|---|---|---|---|
| 2023 | Dato non rappresentativo per elementi non ricorrenti | Circa -$7.3M | Circa $12.0M |
| 2024 | Circa -$15.0M | Circa -$18.3M | Circa $6.5M |
| 2025 | Circa -$8.9M | Circa -$8.3M | Circa $10.7M |
5.3 Storia dei Finanziamenti
Revelation ha fatto ricorso a più finanziamenti per sostenere le operazioni. Questo è normale per una biotech clinical-stage, ma l’impatto sugli azionisti esistenti è stato severo perché il valore di mercato della società è molto ridotto e il prezzo dell’azione è stato sotto pressione.
La storia recente include offering azionarie, strutture con warrant ed esercizi di warrant. Nel febbraio 2024 la società ha annunciato un’offerta pubblica da circa $6,2 milioni. Nel maggio 2025 ha annunciato un’offerta pubblica da circa $4 milioni con azioni e warrant. Nel luglio 2025 ha annunciato un’altra offerta pubblica da circa $5 milioni. Nel gennaio 2026 ha annunciato l’esercizio di warrant per circa $11 milioni di proventi lordi e circa $6,7 milioni di proventi netti.
La capacità shelf registration citata nella ricerca aggiunge un ulteriore livello alla discussione sulla diluizione. Avere una shelf attiva può essere utile perché offre flessibilità nel raccogliere capitale. Per gli azionisti esistenti, però, rappresenta anche potenziale diluizione futura, soprattutto se il capitale viene raccolto a prezzi depressi.
Il modo più pulito per Revelation di migliorare la narrativa finanziaria sarebbe ottenere una partnership, grant, finanziamento non diluitivo o finanziamento strategico meno diluitivo collegato a GEM-AKI. Senza questo elemento, il mercato continuerà a prezzare la probabilità di ulteriore emissione azionaria.
6. Analisi del Titolo e Struttura Azionaria
6.1 Dati di Mercato al 30 aprile 2026
REVB resta una micro-cap estrema. I dataset pubblici mostrano valori leggermente diversi in base al timing, agli aggiornamenti del numero di azioni e al fatto che i cambiamenti collegati ai warrant siano stati recepiti. StockAnalysis riportava una market cap vicina a $4,35 milioni, enterprise value negativo vicino a -$5,70 milioni, 3,72 milioni di azioni e float vicino a 3,27 milioni nello snapshot del 24 aprile 2026. I dati di mercato disponibili il 30 aprile mostravano prezzo intorno a $1,15 e market cap più bassa, circa $3,04 milioni. La differenza va trattata come problema di aggiornamento dati, non come cambiamento della tesi di fondo.
Nota di verifica dati: per micro-cap con reverse split recenti, warrant exercise e conteggio azioni variabile, market cap, float, short interest e cash per share possono differire molto tra provider. L’ultimo filing SEC e le disclosure aziendali vanno controllati prima di ogni aggiornamento futuro.
| Metrica | Valore indicativo / commento |
|---|---|
| Prezzo | Intorno a $1.15 nel controllo del 30 aprile 2026 |
| Market cap | Circa $3.0M-$4.4M a seconda del provider e del conteggio azioni |
| Enterprise value | Negativo nel dataset StockAnalysis |
| Azioni in circolazione | 3.72M nel dataset StockAnalysis del 24 aprile |
| Float | 3.27M nel dataset StockAnalysis |
| 52-week range | Circa $0.99-$40.08 nel dataset citato |
| Performance 52 settimane | Perdita superiore al 96% nel dataset StockAnalysis |
| Media mobile 50 / 200 giorni | Circa $1.25 / $4.90 nel dataset StockAnalysis di aprile |
| Short interest | Dipendente dal provider; basso come percentuale delle shares outstanding nei dataset citati |
| Insider ownership | Circa 4.94% nel dataset StockAnalysis |
| Institutional ownership | Circa 5.35% nel dataset StockAnalysis |
| P/B ratio | Circa 0.21 nel dataset StockAnalysis |
Il dato più evidente è l’enterprise value negativo. In termini semplici, il mercato valuta la società sotto la cassa netta stimata. Per trader speculativi può sembrare attraente, ma in una biotech clinical-stage non è automaticamente bullish. Spesso significa che il mercato sta scontando consumo futuro di cassa, necessità di finanziamento, pressione going concern e potenziale diluizione.
Per REVB, l’enterprise value negativo è meno una chiara anomalia di valutazione e più un segnale di sfiducia. Il mercato sembra dire che la pipeline può avere valore, ma che il percorso per realizzarlo richiede capitale che la società non ha ancora su basi non diluitive.
6.2 Storia dei Reverse Stock Split

Il punto più preoccupante della struttura azionaria è la storia di ripetuti reverse stock split. Un reverse split non distrugge valore da solo, ma quando si ripete insieme a capital raise, emissione di warrant e prezzo dell’azione in calo, diventa il segnale visibile di un ciclo diluitivo.
| Data | Ratio | Motivazione / lettura principale |
|---|---|---|
| Febbraio 2023 | 1-for-35 | Compliance NASDAQ |
| Gennaio 2024 | 1-for-30 | Compliance NASDAQ |
| Gennaio 2025 | 1-for-16 | Compliance NASDAQ |
| Luglio 2025 | 1-for-3 | Compliance NASDAQ |
| Gennaio 2026 | 1-for-4 | Compliance NASDAQ |
Questa sequenza è una red flag strutturale. Non significa che un rally speculativo sia impossibile. Le micro-cap biotech con float ridotto e catalyst reali possono muoversi violentemente. Ma significa che la base azionaria di lungo periodo è stata pesantemente danneggiata, e i nuovi investitori devono capire che il finanziamento futuro potrebbe continuare a pesare sull’equity.
7. Mercato Addressable e Opportunità Commerciale

7.1 Acute Kidney Injury
L’AKI è uno dei bisogni medici insoddisfatti più importanti nella medicina ospedaliera. È comune nei pazienti ricoverati, ancora più comune in terapia intensiva, ed è associato a mortalità, dialisi, permanenza più lunga in ICU, maggiore costo di cura e progressione verso chronic kidney disease. Revelation stima circa 6,8 milioni di pazienti AKI ospedalizzati ogni anno negli Stati Uniti applicando una stima di incidenza del 20% a circa 34 milioni di ricoveri annui.
La società e fonti di mercato terze indicano una grande opportunità commerciale potenziale. Le stime del mercato globale del trattamento AKI variano in base a fonte, metodologia e definizione, ma diversi dataset industriali collocano il mercato in area multi-miliardaria, con crescita attesa fino alla fine del decennio. Per una società della dimensione di Revelation, anche una quota ristretta di un mercato AKI clinicamente validato sarebbe significativa.
L’attrattività commerciale è quindi evidente. Una terapia capace di ridurre morte e/o dialisi in una popolazione AKI definita potrebbe diventare clinicamente ed economicamente rilevante. Potrebbe ridurre carico ICU, uso di dialisi, complicanze e progressione a lungo termine verso CKD. La sfida è altrettanto evidente: l’AKI è stata un’area molto difficile per molte terapie promettenti perché la condizione è eterogenea, acuta, complessa e influenzata da molte comorbidità e variabili ospedaliere.
7.2 Chronic Kidney Disease
La CKD è una popolazione cronica ancora più ampia, con decine di milioni di pazienti solo negli Stati Uniti. Anche il mercato globale dei farmaci per CKD è multi-miliardario e in crescita, spinto da invecchiamento della popolazione, diabete, ipertensione, malattie cardiovascolari e miglioramento della diagnosi.
Per Revelation, l’importanza di breve termine della CKD non è principalmente commerciale. È scientifica. PRIME fornisce evidenza biologica in pazienti reali con malattia renale e sostiene la razionale per testare Gemini in AKI. In futuro, GEM-CKD potrebbe diventare un proprio percorso di sviluppo, ma nell’attuale setup di mercato la CKD funziona soprattutto come proof-of-biology a supporto del programma AKI, che ha impatto potenziale più forte sulla valutazione.
8. Analisi Competitiva
Il panorama competitivo AKI include più di 30 aziende e programmi secondo sintesi di pipeline di terze parti, ma la maggior parte affronta lo stesso problema centrale: tradurre meccanismi biologici plausibili in beneficio clinico chiaro in un setting acuto difficile. Inibizione del complemento, sostituzione della fosfatasi alcalina, peptidi protettivi, modulazione metabolica e strategie anti-infiammatorie sono state tutte esplorate.
| Azienda | Farmaco / programma | Fase indicativa | Meccanismo / focus |
|---|---|---|---|
| AstraZeneca / Alexion | Ravulizumab | Contesto competitivo AKI / Phase 3 | Inibizione complemento C5 |
| AM-Pharma / Kyowa Kirin | Ilofotase alfa | Phase 3 nel panorama AKI storico | Fosfatasi alcalina ricombinante |
| Novartis | TIN816 | Contesto Phase 2b | Approccio renale / infiammatorio |
| Guard Therapeutics | RMC-035 | Phase 2 | Peptide protettivo |
| Arch Biopartners | LSALT peptide | Phase 1b/2 | Peptide anti-infiammatorio |
| Kelifarma | KELI-101 | Contesto Phase 1b/2 | Programma su kidney injury / infiammazione |
| Revelation Biosciences | Gemini / GEM-AKI | Phase 2/3 pianificata | TLR4 agonist / trained immunity / ribilanciamento immunità innata |
La differenziazione di Gemini è che non si limita a bloccare un singolo pathway infiammatorio a valle. Punta invece a ribilanciare a monte l’immunità innata. Questo potrebbe essere un vantaggio se la biologia si tradurrà in protezione ampia in pazienti AKI eterogenei. Potrebbe anche essere un limite se il meccanismo si rivelasse troppo indiretto, troppo variabile tra popolazioni o insufficiente per muovere endpoint clinici duri.
La competizione da parte di aziende più grandi è un rischio importante. Società come AstraZeneca, Novartis o altri sponsor ben capitalizzati hanno maggiore capacità clinica, regolatoria e finanziaria. Se un player più grande producesse dati forti per primo, l’opportunità percepita di Gemini potrebbe ridursi. Al contrario, fallimenti persistenti dei concorrenti manterrebbero aperto l’unmet need e potrebbero rendere un meccanismo differenziato come Gemini più interessante, se Revelation riuscirà a eseguire.
9. Analisi SWOT
Punti di forza
Meccanismo d’azione differenziato. Gemini/PHAD si basa su ribilanciamento dell’immunità innata e trained immunity, non su immunosoppressione ampia classica.
Percorso di sviluppo allineato con FDA. L’accordo di gennaio 2026 su un singolo trial adattivo Phase 2/3 crea una strada potenzialmente efficiente verso NDA se i dati saranno positivi.
Piattaforma multi-indicazione. Lo stesso candidato viene esplorato in AKI, CKD, infezioni post-chirurgiche e prevenzione infezioni in ustioni gravi, creando più potenziali percorsi di valore da una sola piattaforma scientifica.
Dati PRIME incoraggianti. I risultati biomarker CKD e i commenti degli investigator supportano la razionale biologica e danno più sostanza alla storia rispetto a una pura ipotesi preclinica.
Punti di debolezza
Capitalizzazione estremamente ridotta. Una società valutata pochi milioni di dollari deve finanziare un trial clinico complesso che potrebbe richiedere capitale superiore all’attuale valore di mercato.
Storia di diluizione severa. Capital raise ripetuti, strutture con warrant e reverse stock split hanno danneggiato la storia azionaria.
Pressione going concern. Il runway fino al Q1 2027 non elimina la necessità di finanziamento aggiuntivo.
Team interno piccolo. La capacità di eseguire un trial complesso dipende fortemente da CRO e advisor esterni.
Opportunità
Ampio unmet need in AKI. Una terapia che riduca morte e/o dialisi potrebbe avere valore clinico e commerciale significativo.
Potenziale partnership o licensing. Progressi clinici più solidi potrebbero attrarre l’interesse di aziende farmaceutiche o biotech più grandi.
Setup da enterprise value negativo. La valutazione depressa può attirare trader speculativi alla ricerca di asimmetrie biotech.
Espansione pipeline. GEM-PSI e GEM-PBI aggiungono optionalità di lungo periodo se la piattaforma sarà validata.
Minacce
Rischio di fallimento clinico. L’AKI è storicamente difficile, e attività biomarker iniziale potrebbe non tradursi in endpoint clinici.
Competizione da società più grandi. Sponsor meglio finanziati hanno risorse di sviluppo e commerciali superiori.
Rischio compliance NASDAQ e delisting. La storia dei reverse split mostra che la compliance di quotazione è stata un problema ricorrente.
Rischio finanziamento futuro. Capital raise aggiuntivi potrebbero essere molto diluitivi se realizzati a prezzi depressi.
10. Valutazione e Target degli Analisti
La copertura analitica di REVB è molto limitata, coerentemente con lo status di micro-cap della società. I target disponibili variano molto e devono essere letti con cautela. Alcune piattaforme terze mostrano target teorici elevati, ma quei target sono spesso basati su campioni molto piccoli di analisti o su ricerca compensata dall’emittente. Zacks SCR, per esempio, dichiara compensazione dall’emittente per la copertura, elemento che riduce il valore di indipendenza del rating e del target.
| Fonte / dataset | Rating / contesto target | Cautela importante |
|---|---|---|
| Zacks SCR | Target price elevato nella ricerca di gennaio 2026 | Ricerca compensata dall’emittente; da trattare con cautela |
| TradingView consensus | Campione analisti molto limitato | Consensus poco robusto con uno o pochissimi analisti |
| Investing.com / aggregatori | Range target ampio | Da verificare rispetto a conteggio azioni e filing aggiornati |
| Modelli quantitativi / tecnici | Spesso negativi | Riflettono momentum debole e storia di diluizione |
Un approccio più conservativo guarda alla cassa netta per azione, ma questa metrica non è un floor semplice. In una biotech clinical-stage, la cassa viene consumata dal burn operativo e dallo sviluppo clinico. Può inoltre essere controbilanciata da warrant, nuove emissioni azionarie, payables e obblighi di trial. Trattare sotto la cash per share stimata può indicare sottovalutazione, ma può anche indicare che il mercato si aspetta che la cassa venga consumata e che gli azionisti siano diluiti prima che la pipeline crei valore.
Il framework più utile per REVB è quindi scenario-based. In uno scenario di successo GEM-AKI, l’attuale market cap apparirebbe probabilmente troppo bassa rispetto all’opportunità potenziale. In uno scenario di ritardo o diluizione, la valutazione depressa potrebbe essere giustificata o persino ancora troppo alta. Per questo il titolo va analizzato come storia clinica e di finanziamento guidata da catalyst, non come investimento tradizionale basato su multipli.
11. Catalizzatori e Rischi
Catalizzatori positivi da monitorare
Il 2026 è un anno cruciale per Revelation. Il catalyst potenziale più importante è l’avvio formale del trial Phase 2/3 GEM-AKI. Il mercato dovrà vedere conferme pratiche, non solo linguaggio generico: selezione della CRO, attivazione dei siti clinici, aspettative di arruolamento, piano di dosaggio, disponibilità del clinical drug supply, chiarezza regolatoria e pianificazione della cassa.
Altri catalyst includono ulteriori presentazioni dei dati PRIME a conferenze scientifiche, update del management sull’infrastruttura del trial, possibili discussioni di partnership o licensing, risultati trimestrali e qualsiasi nuova struttura finanziaria capace di ridurre le preoccupazioni sulla diluizione. Gli earnings non sono importanti per i ricavi, perché la società non ne ha. Sono importanti perché aggiornano cash balance, burn rate, runway e timeline operativa.
Rischi principali
Il rischio clinico è il più grande. L’AKI è un’area di sviluppo difficile. I pazienti sono eterogenei, il decorso della malattia è acuto, lo standard of care varia tra setting e endpoint come morte e dialisi sono difficili da muovere. Biomarker positivi in Phase 1 o Phase 1b sono incoraggianti, ma non garantiscono efficacia clinica.
Il rischio finanziario è altrettanto critico. La società avrà probabilmente bisogno di capitale aggiuntivo significativo per completare il trial Phase 2/3 pianificato. Se il capitale verrà raccolto tramite equity o strutture pesanti di warrant a prezzi depressi, la diluizione potrebbe restare severa.
Il rischio regolatorio è che le richieste FDA possano evolvere. L’accordo sul pathway è positivo, ma non garantisce che il trial avrà successo, che i dati saranno sufficienti o che la FDA non richiederà ulteriori analisi, informazioni di sicurezza o evidenze confermative.
Il rischio competitivo è che una società più grande possa ottenere dati positivi o approvazione in AKI prima di Gemini, riducendo l’opportunità percepita. Anche se Gemini funzionasse, il posizionamento commerciale dipenderà da label, popolazione, timing, adozione ospedaliera, prezzo ed evidenza comparativa.
Il rischio NASDAQ/listing resta rilevante perché il prezzo dell’azione è ripetutamente sceso in area di pressione sulla compliance. Reverse split ripetuti possono mantenere temporaneamente la quotazione, ma danneggiano anche la fiducia degli investitori e spesso rafforzano la percezione di equity strutturalmente debole.
12. Scenario Bull, Base e Bear
| Scenario | Cosa deve succedere | Implicazione editoriale |
|---|---|---|
| Bull case | Avvio chiaro di GEM-AKI, piano CRO/siti credibile, funding gestibile, nessuna diluizione punitiva immediata, supporto scientifico continuo per PRIME, possibile interesse strategico o partnership. | REVB potrebbe diventare una storia AKI micro-cap altamente speculativa ma credibile, con potenziale di repricing significativo. |
| Base case | La società continua la preparazione del trial, brucia cassa lentamente, raccoglie capitale aggiuntivo su basi diluitive, sopravvive fino ai prossimi update clinici ma non risolve del tutto l’overhang finanziario. | Il titolo resta volatile, con rally sulle news e pressione strutturale tra un catalyst e l’altro. |
| Bear case | Ritardi del trial, capital raise punitivo, ulteriore debolezza azionaria, nuova pressione NASDAQ, update clinici/regolatori deludenti o incapacità di finanziare il programma AKI. | Il rischio di ulteriore distruzione di valore, diluizione e pressione da reverse split resta elevato. |
13. Conclusione
Revelation Biosciences è un caso biotech ad alto rischio e alta optionalità teorica. Da un lato, la società ha costruito una storia scientifica più sostanziosa di molte narrative biotech micro-cap: Gemini ha un meccanismo differenziato, i dati clinici iniziali supportano attività farmacodinamica, il percorso AKI allineato con FDA è potenzialmente efficiente e l’Advisory Board aggiunge credibilità clinica al programma Phase 2/3 pianificato.
Dall’altro lato, i rischi strutturali sono severi. La market cap è estremamente ridotta, la storia di reverse split è difficile, la società non ha ricavi, il linguaggio going concern e i limiti di runway contano, e sarà probabilmente necessario capitale aggiuntivo significativo per completare il programma pivotale AKI. L’enterprise value negativo riflette non solo potenziale sottovalutazione, ma anche profondo scetticismo del mercato sulla capacità della società di trasformare la pipeline in valore senza ulteriore diluizione.
Per trader biotech speculativi, REVB può stare nel radar come micro-cap guidata da catalyst con un concetto AKI insolitamente chiaro. Per investitori conservativi, il profilo di rischio resta incompatibile con un framework prudente. Le variabili decisive nei prossimi mesi sono semplici: finanziamento, avvio formale del trial GEM-AKI, visibilità sull’arruolamento e qualità dei futuri update clinici/regolatori.
Disclaimer: Questo contenuto è fornito esclusivamente a scopo informativo ed educativo e non costituisce consulenza finanziaria, d’investimento, legale, fiscale, medica o di trading. Non è una raccomandazione di acquisto, vendita o detenzione di alcun titolo. Le società biotecnologiche in stadio clinico comportano rischi elevati, inclusi fallimento clinico, ritardi regolatori, diluizione, rischio di delisting e possibile perdita totale del capitale investito. I lettori devono svolgere la propria due diligence e consultare professionisti qualificati prima di prendere decisioni finanziarie.
Reference Sources / Fonti
- Revelation Biosciences official website
- Revelation Biosciences Pipeline
- Revelation Biosciences Management
- Revelation reaches agreement with FDA on Gemini approval pathway for AKI, January 21, 2026
- Revelation announces Acute Kidney Injury Advisory Board, April 6, 2026
- Revelation presents additional positive data from PRIME, March 30, 2026
- PRIME top-line results, September 2025
- Phase 1 Gemini safety and biomarker activity
- 2025 financial results, February 26, 2026
- Warrant exercise for $11 million gross proceeds, January 23, 2026
- Gemini for infection prevention in severe burn patients, April 29, 2025
- SEC EDGAR company filings: Revelation Biosciences, Inc.
- StockAnalysis REVB statistics and valuation dataset
- Yahoo Finance REVB profile
- Frontiers in Immunology: TLR agonists and trained immunity
- Zacks SCR note on REVB, January 2026
Scanner for active traders

Try ChartsWatcher free, then unlock 10% OFF with SAVE10
ChartsWatcher is a real-time scanner for momentum traders: fast movers, unusual volume and rotations — so you can focus on the few tickers that matter right now, instead of watching hundreds of charts.
Start with the free version. When you upgrade, use SAVE10 for 10% OFF your first paid period.
Start free – then use SAVE10
No credit card required to start. Apply SAVE10 when upgrading.
Recommended platform

One platform. All your brokers.
Medved Trader connects multiple brokers in one workspace, with pro charts, hotkeys and fast execution — without changing your broker accounts.
A single cockpit for positions, Level II and multi-broker order routing, built for active day & swing traders.
Get 1 Month Free ➔
Multi-broker workflow + customizable layouts in one platform.


